Les syndromes cardio-rénaux
L’œuf ou la poule revisités. Parfois, c’est compliqué!
Entre les deux mon cœur balance.
=>Une évolution conceptuelle
Dr Maxime HOFFMANN
Hôpitaux privés La Louvière (Lille) et de Villeneuve d’Ascq.
Introduction.L’insuffisance cardiaque (IC) est un problème majeur de santé publique des pays occidentaux. La prévalence en France de l’ insuffisance cardiaque était estimée sur les données de registre de 2022 à 1,4 millions de patients, soit environ 2,6% de la population adulte. Elle est responsable de 24645 décès en 2022 et est la source d’une altération de la qualité de vie notamment en raison des symptômes invalidants induits, des pathologies associées et des hospitalisations fréquentes (1).Le terme de syndrome cardio rénal a été utilisé la première fois en 1988 par Al Khalder désignant une situation clinique et physiopathologique restreinte: une altération de la fonction rénale secondaire à une baisse du débit cardiaque en rapport avec une situation chronique d’insuffisance cardiaque (2). En 2010, Ronco élargit le concept qui désigne désormais une entité physiopathologique complexe touchant le cœur et les reins dans laquelle la dysfonction aiguë ou chronique d’un des organes peut induire une dysfonction aiguë ou chronique de l’autre organe –et en définit 5 types (3). Plus récemment, dès 2013 mais surtout à partir de 2018, apparait le terme de «syndrome cardiorénal et métabolique», un peu différent que nous expliciterons à la fin de cet exposé (4,5).I. Approche classique en 5 stades (6,7)
L’apparition d’une atteinte rénale au cours de l’insuffisance cardiaque définit le syndrome cardio-rénal (SCR).Ronco en propose 5 types:
• Type 1 : syndrome cardio-rénal aigu
• Type 2 : syndrome cardio-rénal chronique
• Type 3 : syndrome réno-cardiaque aigu
• Type 4 : syndrome réno-cardiaque chronique
• Type 5 : syndrome cardio-rénal secondaire
On estime que 30% des patients hospitalisés pour décompensation cardiaque ont une élévation de créatininémie de plus de 3 mg/l au cours de leur séjour. Environ 35% des insuffisants cardiaques ont un eDFG (estimé par la formule MDRD) inférieur à 60mL/min/1,73m2 .
L’insuffisance rénale (IR) est un marqueur prédictif fort du pronostic de l’IC. Le risque relatif (RR) de mortalité augmente avec la sévérité de l’insuffisance rénale. Pour un eDFG inférieur à 44 mL/min/1,73m2, ce RR est de 2,85.
Les mécanismes physiopathologiques sont multiples et comprennent généralement:
• une Susceptibilité aux agressions (notamment en cas de néphropathie ischémique ou diabétique sous-jacente)
• une Atteinte inflammatoire chronique (liée aux phénomènes apoptotiques et fibrosants consécutifs à l’atteinte cardiaque)
• une Atteinte hypoxique par diminution de la pression de perfusion (bas débit cardiaque et hyperpression veineuse centrale)
• (une Toxicité médicamenteuse hémodynamique ou lésionnelle (IEC, diurétiques, produit de contraste iodé, AINS).
Les conséquences cliniques sont nombreuses et lourdes:
• Syndrome de résistance aux diurétiques
• Iatrogénie accrue avec risque de sous médication
• Augmentation du risque cardio-vasculaire global
Les atteintes aiguës correspondant aux types 1,3 et 5 de SCR seront peu abordées ici. Elles concernent en général peu le médecin généraliste et relèvent plus d’une pratique de service de soins intensifs cardiologiques ou néphrologiques, avec des pathologies plus lourdes, et propres à ces services, tant en monitorage invasif (pressions centrales) qu’en surveillance biologiques ou échocardiographiques régulières. C’est dans ces types que l’ on rencontre en général les formes les plus graves, notamment le syndrome de resistance aux diurétiques, à savoir l’absence d’obtention d’une diurèse efficace sous une monothérapie de diurétiques et la nécessité de recours à des techniques de ventilation spécifiques ou de la dialyse.
Le SCR de type 1 est caractérisé par une altération aiguë de la fonction cardiaque entraînant une dysfonction rénale aiguë.
Les étiologies sont les suivantes :
• décompensation dans le cadre d’une insuffisance cardiaque sous-jacente ;
• syndrome coronarien aigu ;
• choc cardiogénique ;
• chirurgie cardiaque.
Le syndrome cardio-rénal de type 3 ou réno-cardiaque est caractérisé par une altération aiguë de la fonction rénale entraînant une dysfonction cardiaque aiguë.
Les étiologies classiquement retenues sont :
• néphropathie au produit de contraste ;
• néphrotoxique ;
• chirurgie majeure ;
• chirurgie cardiaque ;
• glomérulonéphrite post-infectieuse ;
• rhabdomyolyse ;
• pyélonéphrite aiguë ;
• néphropathie obstructive
Le SCR de type 5 est caractérisé par l’association d’une insuffisance rénale et d’une insuffisance cardiaque secondaires à une pathologie systémique aiguë ou chronique. La situation la plus fréquente d’atteinte systémique aiguë responsable d’un SCR de type 5 est le sepsis. Parmi les atteintes secondaires, on retrouve le diabète, l’amylose ou encore les vascularites.
Les atteintes chroniques en revanche concernant plus le médecin généraliste et sont constituées des types 2 et 4.
Ces deux types de SCR posent un problème de défi diagnostique et thérapeutique pour le médecin généraliste qui en général ne sait pas par quel bout le prendre:
• comment faire la différence entre une IRA fonctionnelle, par exemple liée à un excès de traitement diurétique et une IRA «congestive», devant justifier à l’inverse d’une titration des diurétiques ?
• Qui traiter à domicile? Qui référer?
• Comment les surveiller après la décompensation?
Le syndrome cardio-rénal de type 2 est caractérisé par des anomalies chroniques de la fonction cardiaque qui entraînent une dysfonction rénale chronique. Les anomalies cardiaques retrouvées dans ce sous-type de syndrome cardio-rénal regroupent :
• l’insuffisance cardiaque chronique ;
• la fibrillation atriale ;
• les cardiopathies congénitales ;
• les péricardites constrictives
• les cardiomyopathies ischémiques
Du point de vue physiopathologique, une situation de bas débit rénal chronique s’installe. Toutefois, son mécanisme reste hypothétique : en effet, il ne semble pas y avoir de corrélation directe entre la fraction d’éjection ventriculaire gauche et la baisse du DFG. Dans une étude hémodynamique regroupant près de 200 patients, seules les pressions de remplissage dans l’oreillette droite étaient plus élevées chez les patients avec une dysfonction rénale plus sévère, indiquant que le facteur congestif est peut- être prédominant dans cette situation clinique.
L’objectif principal de la prise en charge du syndrome cardio-rénal de type 2 reste la prévention de l’apparition de l’insuffisance rénale. Dans un 1er temps, en limitant les agressions rénales secondaires. Par conséquent, l’utilisation des thérapeutiques classiques dans l’insuffisance cardiaque devra se faire avec prudence (par exemple : diurétiques et hypovolémie, bloqueurs du SRAA et hypotension) afin de ne pas aggraver les processus physiopathologiques vus précédemment. Dans un 2nd temps, en luttant contre la congestion rénale. L’utilisation des diurétiques joue alors un rôle central dans la stratégie thérapeutique.
Le SCR de type 4 correspond à une insuffisance rénale chronique primitive responsable d’une dysfonction cardiaque chronique secondaire (remodelage cardiaque, dysfonction diastolique du VG, hypertrophie ventriculaire gauche) et/ ou une augmentation du risque cardio-vasculaire.
Physiopathologiquement, des facteurs tels que l’hypertension artérielle ainsi que l’insuffisance rénale per se conduisent à une hypertrophie ventriculaire gauche, à une dysfonction diastolique et à une augmentation des événements cardiovasculaires. Malgré tous ces éléments, les patients insuffisants rénaux sont en général moins bien pris en charge sur le plan de leurs facteurs de risque en raison de la clairance diminuée des médicaments, du risque augmenté de saignements et des craintes quant aux effets potentiellement délétères (et infondés) des thérapies (comme les bloqueurs du SRAA) sur l’évolution de la fonction rénale. L’anémie, la malnutrition et l’inflammation chronique retrouvées dans la maladie rénale évolutive sont aussi largement incriminées dans la progression des maladies cardiovasculaires.
Dans ce type de syndrome, les principes du traitement sont une association thérapeutique conduisant à une baisse du risque cardio-vasculaire ou des épidoses d’insuffisance cardiaque. Quelques études anciennes ont montré l’intérêt de diverses molécules mais, en dehors des IEC/ARA2, avec des preuves limitées sur la réduction de mortalité.
L’étude IDNT (Irbesartan Diabetic Nephropathy Trial) a également été conçue pour évaluer les effets réno-pro- tecteurs de l’irbésartan par rapport à l’amlodipine ou un placebo chez plus de 1 700 patients. Les résultats ont montré que le groupe irbésartan avait une incidence plus faible d’insuffisance cardiaque par rapport aux groupes amlodipine et placebo. L’utilisation de bêta-bloquants avec des IEC ou des ARA II est associée à un meilleur pronostic cardiovasculaire et rénal chez les personnes âgées et les patients en IR chronique avancée. Dans l’étude EVOLVE (Evaluation of Cinacalcet Hydrochloride Therapy to Lower Cardiovascular Events), une réduction du nombre de 1er épisode d’insuffisance cardiaque a été rapportée dans le groupe cinacalcet. Di Lullo et al. ont constaté que le traitement de patients en pré-dialyse avec du chlorhydrate de sévélamer (1 600 mg/j), permet à la fois de réduire les calcifications des valves cardiaques et de retarder le déclin de la fonction rénale. La correction de la dyslipidémie représente un autre objectif fondamental à atteindre dans la gestion des maladies cardiovasculaires chez les patients insuffisants rénaux chroniques. L’étude SHARP portant sur l’utilisation des statines chez les patients insuffisants rénaux chroniques montre un bénéfice significatif de la combinaison simvastatine/ézétimibe sur l’athérosclérose, mais pas d’impact sur la mortalité totale. Plus récemment, on évoquera bien-sûr les grands essais des gliflozines dans la MRC (DAPA CKD, EMPAKIDNEY) et des agonistes du glp1 (essai FLOW) avec des résultats plus solides y compris sur les critères de mortalité.
II. Vers une vision unificatrice: le syndrome cardio-rénal et métabolique
Le modèle classique «temporel» de Ronco, s’il possède quelques qualités descriptives et didactiques évidentes, est aujourd’hui remis en cause.
En effet, il ne repose sur aucune base de physiopathologie spécifique propre, exceptée la part de surcharge hydrosodée chronique. Il n’a surtout débouché sur aucune avancée de recherche fondamentale ou thérapeutique majeure (8).
De surcroit, Halimi (9) dans une étude de registre portant sur 385687 patients porteur d’un SCR concluait au fait que la distinction entre événement rénal apparaissant avant ou après l’événement cardiaque ne modifiait que très peu le risque CV et rénal. Quel que soit le sous type de SCR, le risque de décès toute cause restait supérieur à 60% à 5 ans.
L’HTA, le diabète, l’obésité ou l’ischémie d’organes sont des paramètres communs à l’IC et à l’IR. Ils aboutissent tous à une fibrose cardiaque, vasculaire et rénale dont la prévention est majeure en réduisant les processus d’ischémie-reperfusion, de stress oxydatif et d’inflammation. Cela a débouchésur un Plaidoyer de l’AHA en 2023 pour une approche thérapeutique globale, devant concerner tous les patients à risque et non plus seulement les patients en IC.
Le syndrome cardiorénal et métabolique (ou CKM syndrome pour cardiac kidney metabolic syndrome des Anglo-Saxons) suppose qu’en cas d’anomalies métaboliques, notamment en cas d’adiposité dysfonctionnelle, il y a un risque de diabète de type 2 et d’événements cardiaques et rénaux qui peuvent être prévenus par une approche thérapeutique spécifique, holistique, d’association de classes thérapeutiques permettant de réduire de façon complémentaire les évenements cardiaques et rénaux. Dès lors, est-il possible pour autant de prévenir les événements athéro thrombotiques, l’insuffisance cardiaque (IC) et la maladie rénale chronique (MRC) avec une même stratégie thérapeutique?
Sur l’étude de la littérature (10), une réponse commence à se dégager mais l’analyse critique formelle multi-critères appelle toujours à la prudence notamment si on prend en compte tous les effets suivants:
• L’ effet classe: toutes les molécules d’une même classe pharmacologique, lorsqu’elles sont appliquées à une même situation clinique, produisent-elles les mêmes effets bénéfiques et les mêmes effets indésirables?
• L’effet groupe: un groupe thérapeutique, i.e. un ensemble de classes thérapeutiques agissant sur une même cible donnée ou critère intermédiaire (PA, glycémie, LDLc…), produit-il un bénéfice clinique proportionnel à l’action sur ce critère et indépendant du moyen utilisé?
• L’effet croisé: le traitement (ou la prévention d’une maladie, par exemple l’IDM) rend-il possible la prévention de la survenue d’une autre maladie (par exemple un AVC ou une MRC)?
A ce jour, il convient de raisonner plutôt en termes de bénéfices cliniques croisés en certaines circonstances, plutôt encore qu’en terme de continuum CRM.
Les études ponctuelles et factuelles existent par exemple avec les gliflozines et les aGLP1 mais uniquement dans certaines circonstances et pour certains critères (essais DAPA CKD, EMPAKIDNEY, FLOW par exemple). Même si cela apparait tentant de le penser, les essais actuels ne permettent à ce jour pas de conclure «scientifiquement» et stricto sensu sur l’extension de l’indication de ces molécules dans tout le continuum cardio-métabolique.
Cela n’est toutefois pas une raison pour ne pas agir et ne pas méconnaître les circonstances particulières lors desquelles les patients ne doivent pas être «sous-traités».
Ainsi, chez un patient ayant un diabète de type 2, il est indispensable de savoir s’il est en prévention CV secondaire, s’il a une IC, s’il a une MRC ou s’il est à risque CV. Dès lors qu’il répond à l’une de ces conditions, son traitement doit comprendre prioritairement au moins une gliflozine et/ou un ar-GLP1 en fonction de la situation clinique. En cas d’antécédent d’AVC, un ar-GLP1 sera prioritaire; en cas de MRC, une gliflozine sera prioritaire.
De la même façon, en l’absence de DT2, là aussi, il est possible d’obtenir des bénéfices cliniques croisés :– en cas de MRC (DFG inférieur à 45 mL/min/1,73 m2 ou un RAC supérieur à 200 mg/g) ou en cas d’IC, quelle que soit la valeur de la FEVG, prescrire une gliflozine, en sus d’un IEC ou un ARA2, préviendra la MRC et l’IC et diminuera leur risque d’évolution ;– en cas d’obésité, en prévention CV secondaire, un ar-GLP1 à forte dose diminuera le risque d’événements athérothrombotiques, de MRC et d’IC.
Si l’on a raisonné pendant des années sur des critères intermédiaires (PA, glycémie, LDLc…), l’histoire récente de la prévention, primaire ou secondaire, justifie desormais de raisonner en fonction de situations cliniques et des effets connus des traitements disponibles, et sur des données solides de prévention d’événements cardio-vasculaires et rénaux et de réduction de la mortalité.
Conclusion.
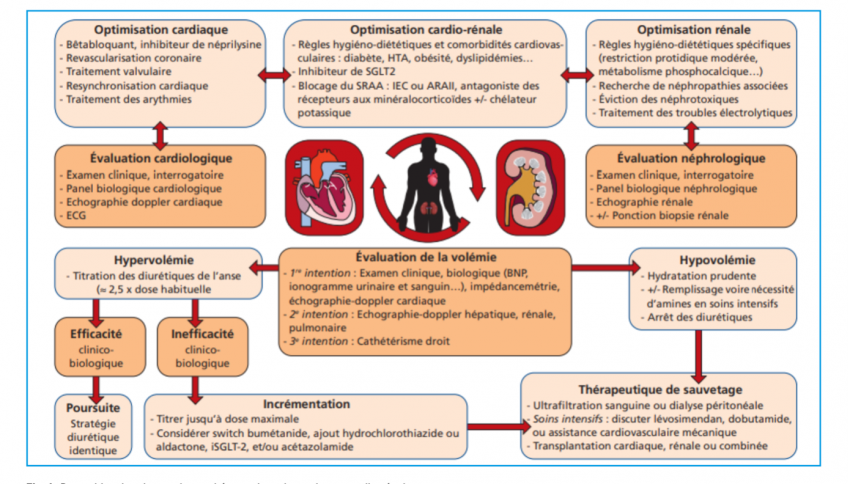
Au-delà de ces concepts très théoriques, on conclura chez le patient porteur d’une IC et développant une IR sur la nécessité pour le médecin généraliste d’une bonne évaluation clinique du patient, basée sur la recherche classique des facteurs de précipitation de l’IR (obstacle, exposition à des médicaments perturbant l’hemodynamique intra-rénale, pertes digestives) et la nécessaire évaluation de la surcharge hydrosodée (prise de poids notamment) qui guidera sa prise en charge et qui est résumée dans l’image 1.
Références
(1) Gabet et al, Epidemiology of heart failure in France. Arch Cardiovasc Dis 2024
(2) Al Kader. The cardio-renal syndrome. Nephron. 1988
(3) Ronco et al, Cardio renal syndromes. Curr Opin Crit Care. 2009
(4) Hatamizadeh et al, Cardiorenal syndrome. Nat Rev Nephrol 2013
(5) Zannad et al, Cardiorenal syndrome revisited. Circulation 2018
(6) Michel et al, Le syndrome cardio-rénal. Conférence d’actualisation -SFAR 2017
(7) Abdelbaki et al, Le syndrome cardio rénal. Réalités cardiologiques 2024
(8) Halimi, Le syndrome cardio rénal et métabolique : un concept unificateur qui a de l’avenir. Correspondance en CRM 2024
(9) Halimi et al, Long term impact of cardio renal outcomes. Nephrol Dial Transplant 2022
(10) Dievart, Les maladies cardiaques, rénales et métaboliques forment-elles un continuum thérapeutique ? Réalités cardiologiques 2025
Présentation lors du congrès : 
